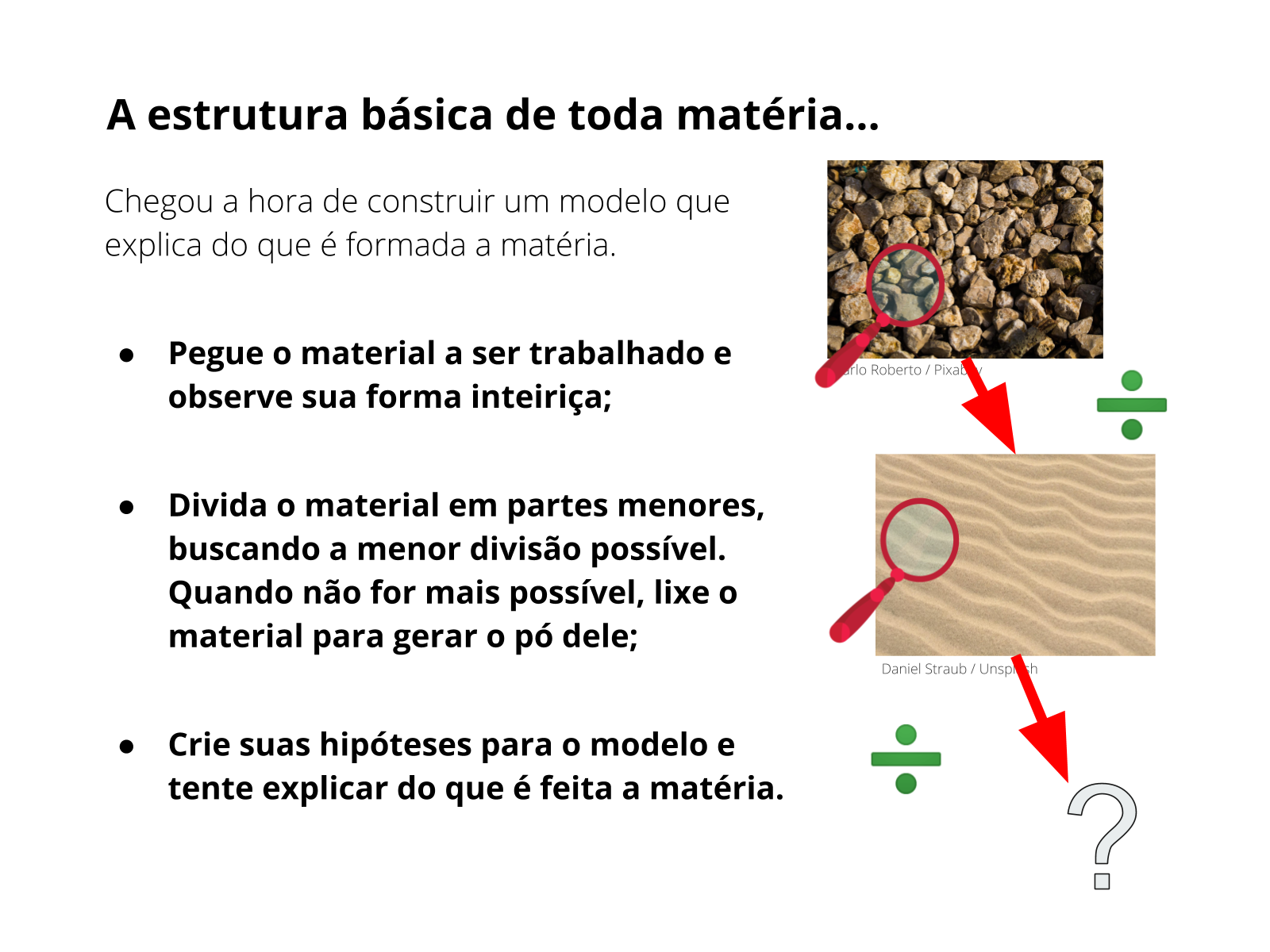
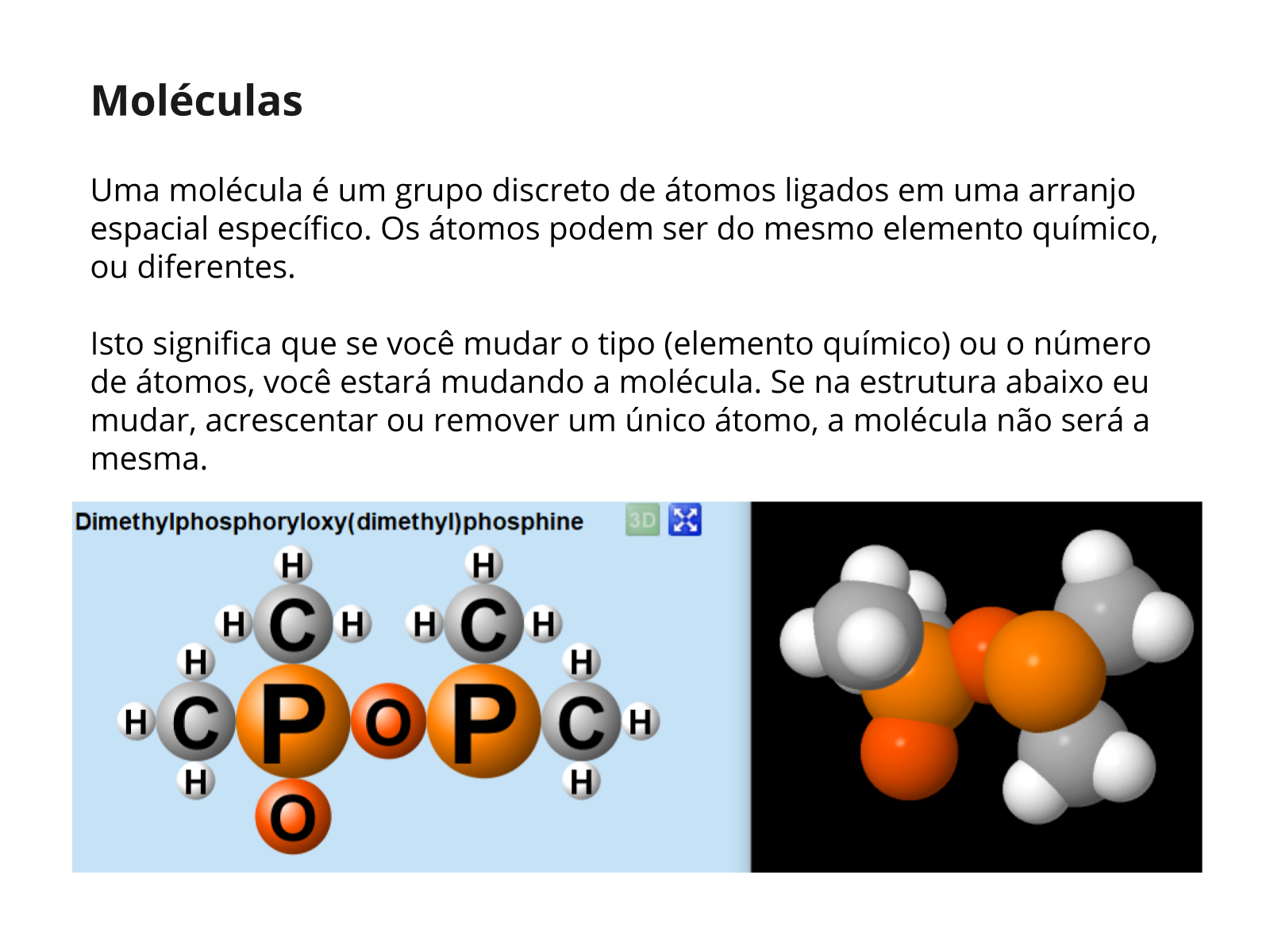
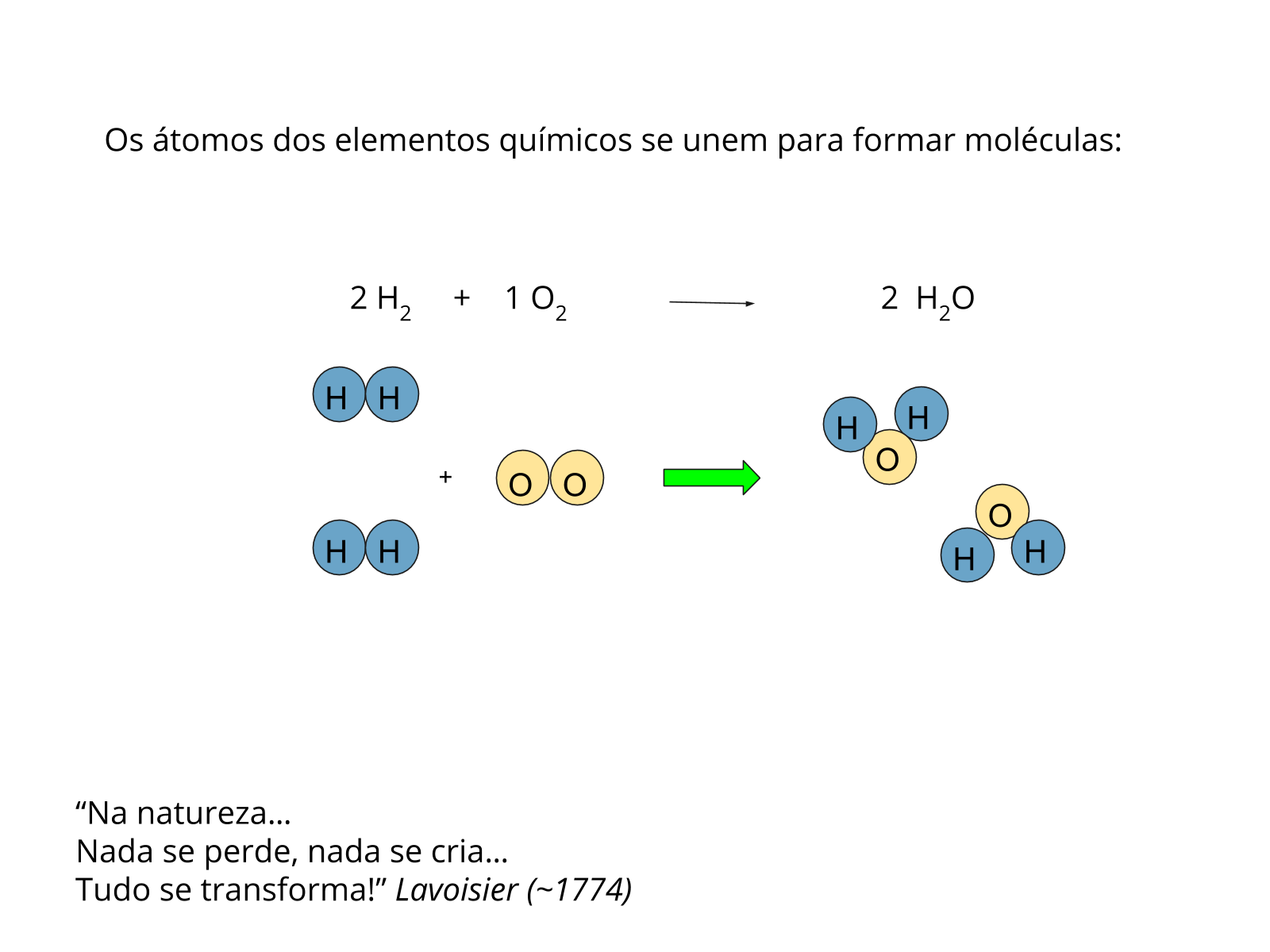
Atividade para impressão - parte 1 - Do que é composto o átomo?
Plano de Aula
Plano de aula: Ensinar modelos que descrevem a estrutura do átomo
Plano 3 de uma sequência de 5 planos. Veja todos os planos sobre Estrutura da matéria
Tem interesse no tema "Neurociência, adolescências e engajamento nos Anos Finais"?
Inscreva-se neste tema para receber novidades pelo site e por email.
Habilidades BNCC:

Precisa de ajuda para criar uma aula personalizada?
Crie seu plano de aula em menos de um minuto no WhatsApp.
Novo curso gratuito

Conheça nosso mais novo curso sobre adolescências, neurociência e engajamento nos anos finais
VER CURSO