Atividade para impressão 1
Plano de Aula
Plano de aula: Pureza de reagentes e produtos
Plano 5 de uma sequência de 5 planos. Veja todos os planos sobre Aspectos quantitativos das transformações químicas
Sobre este plano

Este slide não deve ser apresentado para os alunos, ele apenas resume o conteúdo da aula para que você, professor, possa se planejar.
Sobre esta aula: Para o pleno desenvolvimento desse plano, é essencial que os alunos tenham construído e desenvolvido habilidades
referente aos quatro planos anteriores, desta unidade, sobre as leis ponderais (Conservação das Massas e das Proporções Constantes), reações de combustão (rearranjo dos átomos durante uma reação química) e interpretação e balanceamento de equações químicas. Este plano é uma síntese das habilidades e conceitos desenvolvidos e aplicados para o fechamento desta unidade.
Este plano tem por objetivo possibilitar aos alunos que observem, a partir de tabelas e gráficos, a composição percentual dos componentes que são encontrados em materiais, substâncias e regentes de uma reação químicas. Ao fim deste planos os alunos deverão ser capazes de interpretar e identificar impurezas como componentes indesejados em uma amostra, comprometendo suas propriedades e, consequentemente, suas aplicações.
Para o desenvolvimento deste plano, serão realizadas duas atividades para impressão, que podem ser acessadas através dos links a seguir:
Atividade 1:
Atividade 2:
O gabarito das atividades pode ser acessado através dos links:
Gabarito da atividade 1:
Gabarito da atividade 2:
Para estudar mais sobre o assunto, o professor pode acessar as seguintes referências:
FOGAÇA, Jennifer Rocha Vargas. “Cálculos estequiométricos com reagentes impuros”. Mundo Educação. Disponível em: <https://mundoeducacao.bol.uol.com.br/quimica/calculos-estequiometricos-com-reagentes-impuros.htm>. Acesso em 12 de agosto de 2018.
FOGAÇA, Jennifer Rocha Vargas."Aço"; Brasil Escola. Disponível em <https://brasilescola.uol.com.br/quimica/aco.htm>. Acesso em 12 de setembro de 2018.
MIODOWNIK, Mark. De que são feitas as coisas. Tradução de Marcelo Barbão. Editora Edgard Blücher Ltda., 2015. 34 p.
Materiais necessários para a aula: Apenas materiais para impressão serão utilizados para esta aula:
Atividade 1:
Atividade 2:
Gabarito da atividade 1:
Gabarito da atividade 2:
Título da aula

Tempo sugerido: 2 minutos
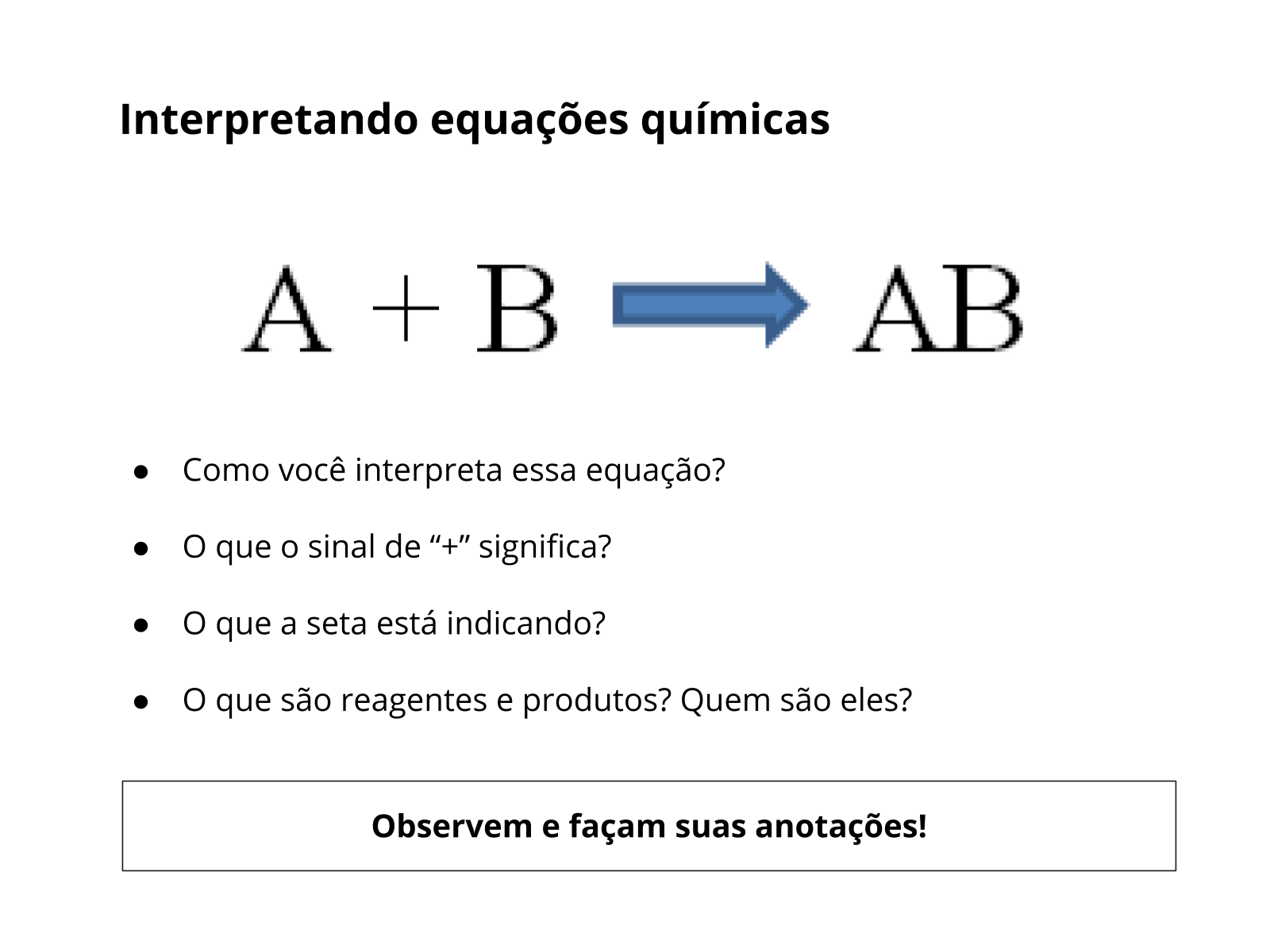
Orientações: Leia o título da aula para a turma, fazendo as seguintes perguntas para relembrar conceitos de aulas anteriores:
- O que são reagentes?
- O que são produtos?
- O que significa pureza de reagentes e produtos?
Como já trabalhado em planos anteriores, os alunos devem responder que reagentes são as substâncias que são misturadas em uma reação química para formar uma nova substância, o produto, através do rearranjo de seus átomos.
A pureza de um reagente ou do produto indica o quanto deste reagente (porcentagem) é realmente a substância em questão. Na Natureza, é muito raro encontrar alguma substância na sua forma pura. A maioria dos produtos é encontrada na forma de misturas. Quando falamos que determinada substância tem 80% de pureza em massa, significa que 80% da massa do produto é da substância em questão e 20% de impurezas.
Contexto

Tempo sugerido: 7 minutos
Orientações: Leia o título da reportagem para os alunos e faça a seguinte pergunta:
- De que material uma espada de samurai é feita?
Provavelmente, a maioria dos alunos irá responder que a espada é feita de metal (nesse caso, pergunte qual o metal), de ferro, de aço etc.
O professor pode auxiliar os alunos com as seguintes dicas de aplicações :
- O material é utilizado em panelas; talheres; rodas de automóveis; pregos; construção civil (no concreto armado).
Os alunos devem chegar à conclusão de que esse material, com vastas aplicações, é o aço. A seguir serão descritos alguns trechos do livro “De que são feitas as coisas” do professor Mark Miodownik, a respeito da fabricação de espadas pelos samurais. Leia para a turma, ou peça para que um dos alunos leia para toda a classe (você pode imprimir o texto, caso julgue necessário):
“Por volta do século XV, a espada de aço feita pelos samurais do japão era a melhor que o mundo já tinha visto e permaneceria preeminente por quinhentos anos até o advento da metalurgia como uma ciência no século XX. Essas espadas eram feitas de um tipo especial de aço, feito da areia negra vulcânica do Pacífico (que consiste principalmente de um minério de ferro chamado magnetita, o material original da agulha das bússolas). Esse aço é feito em um enorme recipiente de barro (espécie de forno). O recipiente é “incendiado” por um fogo aceso dentro dele. Depois de incendiado, é empacotado meticulosamente com camadas de areia negra e carvão vegetal, que são consumidos na fornalha de cerâmica.”
“O processo demora em torno de uma semana e exige atenção constante de uma equipe de quatro ou cinco pessoas para garantir que a temperatura do fogo seja mantida alta o suficiente. No final, o aço é retirado das cinzas e remanescentes da areia e do carvão vegetal. Ninguém poderia criar aço mais forte e mais duro que os samurais antes da revolução industrial.”
A referência completa pode ser encontrada a seguir:
MIODOWNIK, Mark. De que são feitas as coisas. Tradução de Marcelo Barbão. São Paulo: Editora Blücher, 2015. 34 p.
Para mais detalhes sobre a fabricação da espada samurai, o professor pode seguir o link da reportagem a seguir:
“Como é é feita uma espada de samurai”. BBC. Disponivel em: <https://www.bbc.com/portuguese/geral-42959015>. Acesso em 13 de agosto de 2018.
O professor pode complementar essa etapa, comentando que o aço é uma liga metálica (uma mistura de metais), composta por aproximadamente 98,5% de ferro (que vem do minério) e 0,2 a 1,7% de carbono (que vem do carvão). A porcentagem exata de carbono deve ser respeitada, pois aços com alto teor de carbono acabam por se tornar frágeis, não sendo adequados para a produção de uma boa espada, pois sua lâmina quebraria facilmente durante uma batalha. Esse é um dos motivos pelo qual o processo de fabricação de espadas era demorado e meticuloso.
O professor pode fazer a seguinte pergunta para finalizar o contexto:
- O aço é um material puro? Por quê?
Permita que os alunos desenvolvam seus argumentos a respeito das informações e do debate inseridos na sala. Eles deverão ser capazes de dizer que não, já que é uma liga e, portanto, formado por uma mistura de substâncias (o ferro e o carbono).
Questão disparadora

Tempo sugerido: 2 minutos
Orientações: Leia a questão disparadora e faça a seguintes perguntas para auxiliar os alunos:
- O que torna uma substância pura?
- Qual a diferença entre pureza e impureza?
- Existem substâncias puras na Natureza?
Permita que os alunos promovam seus argumentos e desenvolvam hipóteses a fim de realizar um debate sobre o tema em aula.
Lembre que substância pura é aquela formada por um único composto químico, e que impurezas são as substâncias que estão misturadas e não são desejadas (ou porque prejudicam as propriedades dos produtos ou porque atrapalham nas reações químicas). Na Natureza a grande maioria das substâncias e materiais é encontrada na forma de misturas.
Mão na massa
Tempo sugerido: 30 minutos
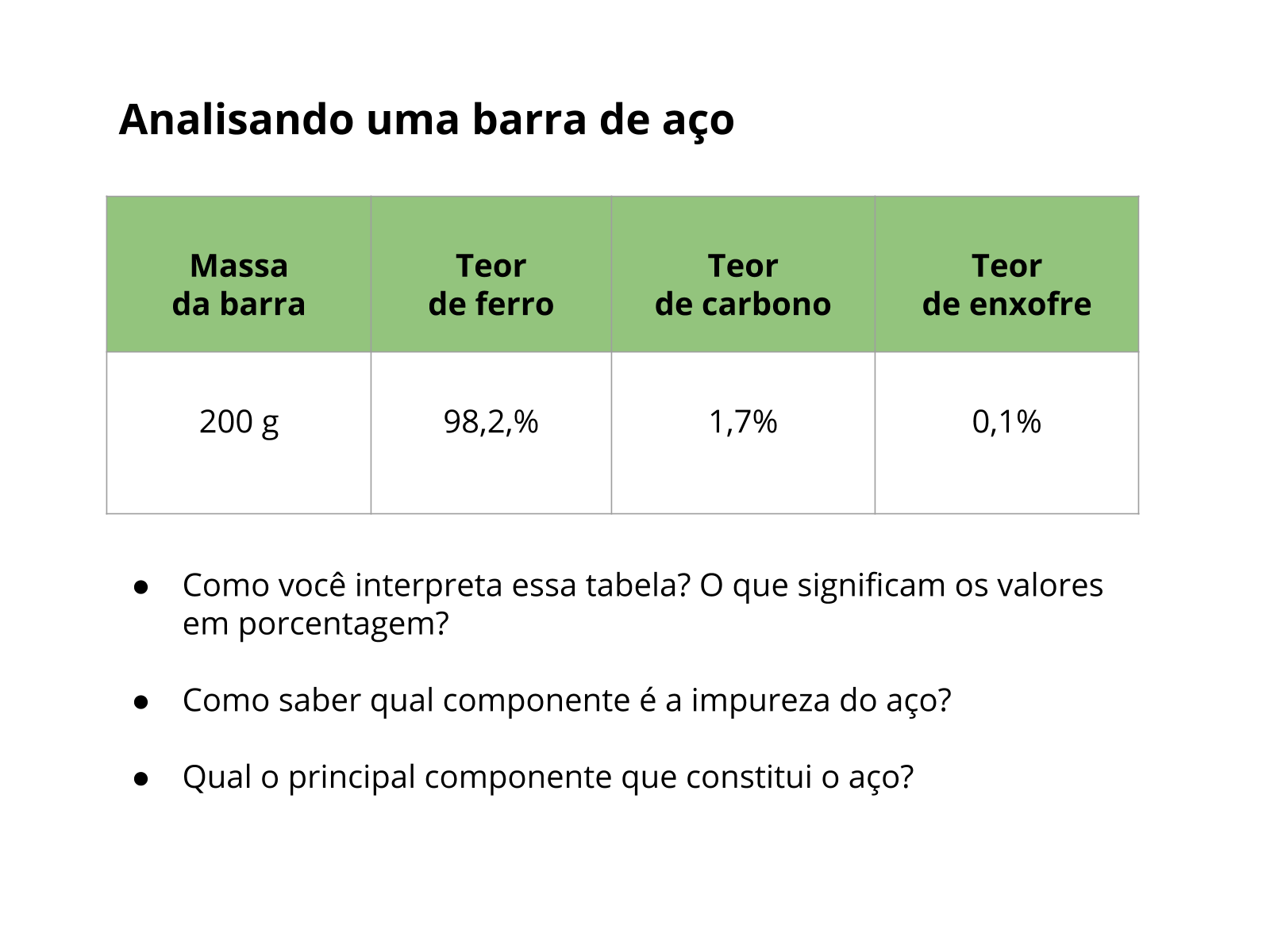
Orientações: Peça aos alunos que formem pequenos grupos para dar início às atividades. Projete o slide, distribua uma cópia impressa para cada grupo ou escreva a tabela, juntamente com seus dados, no quadro. Dê cerca de 3 minutos para que os alunos possam trocar ideias e debater sobre as questões, onde devem chegar até as seguintes conclusões:
1º) A tabela mostra que 200 g de uma barra de aço possui uma composição de 98,2% em ferro, 1,7% em carbono e 0,1% em enxofre.
2º) O enxofre é o componente em menor proporção na composição do aço, uma liga entre ferro e carbono, caracterizando-se como impureza.
3º) O ferro é o principal componente constituinte do aço: 98,2 % da massa de uma barra de aço é de ferro.
Materiais necessários para a aula: Apenas materiais para impressão serão utilizados para esta aula:
Atividade 1:
Atividade 2:
Gabarito da atividade 1:
Gabarito da atividade 2:
Mão na massa
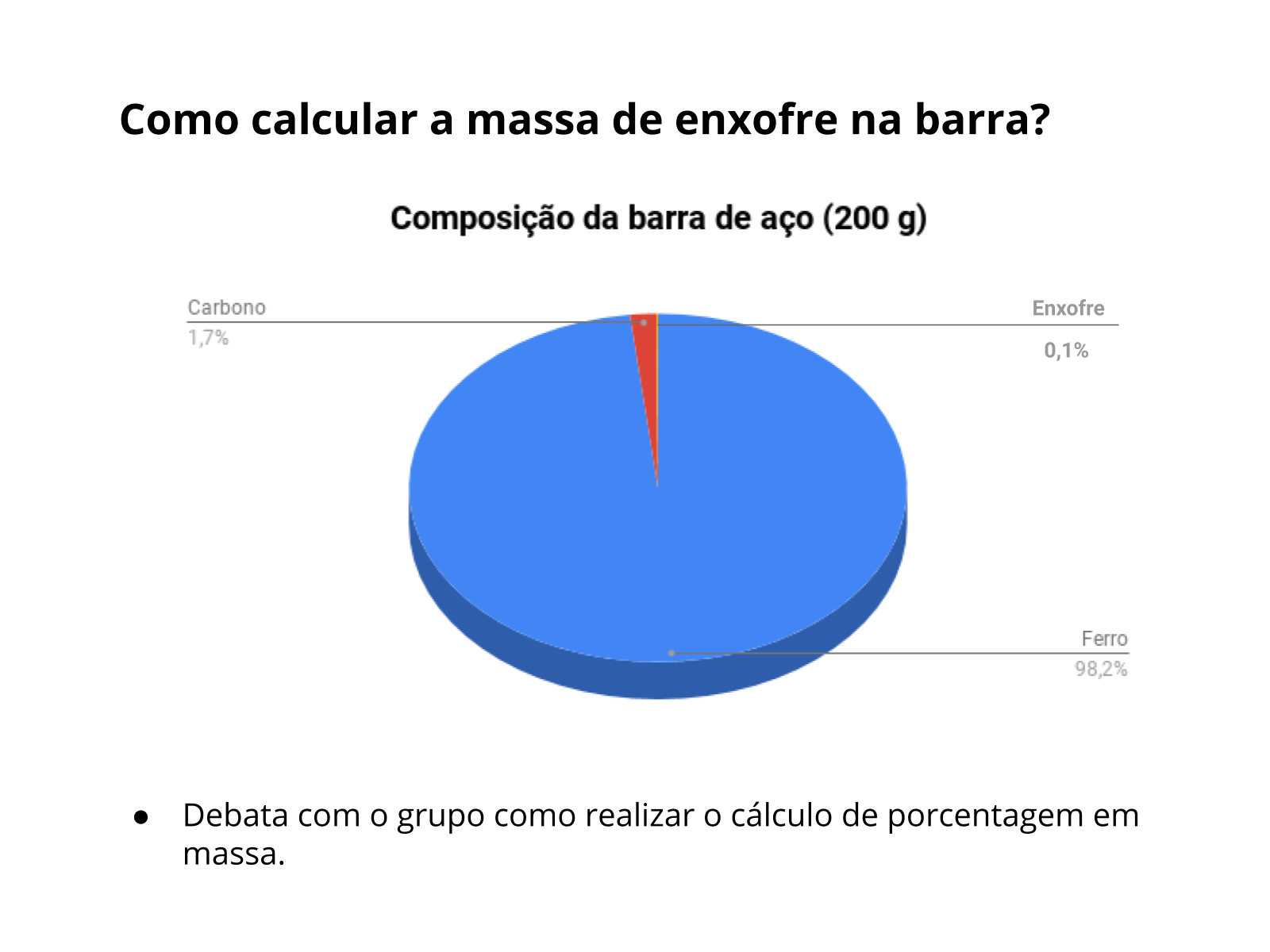
Orientações: Projete o slide. Imprima uma cópia para cada grupo ou desenhe o gráfico no quadro.
Nessa etapa, os alunos devem calcular a massa de enxofre presente na barra de aço. Faça as seguintes perguntas referentes ao gráfico do slide:
- Qual a massa total da barra de aço?
- Qual o valor em porcentagem dessa massa?
- 0,1% corresponde a quantas partes (unidades)?
Caso os alunos tenham dificuldades em determinar a massa de enxofre a partir de sua composição percentual, o professor deve mediar e auxiliar os grupos nesta etapa (tempo sugerido para esta etapa: 7 minutos). Os grupos devem chegar às seguintes conclusões:
- A massa total da barra corresponde a 200 g.
- 200 g (massa total) corresponde a 100% da massa total da barra.
- 0,1% corresponde a 0,1 unidades em 100 unidades.
Para calcular a massa de enxofre na barra, deve-se seguir os passos abaixo:
1º) 0,1% (em massa) corresponde a 0,1 g de enxofre em 100 g da amostra total.
2º) Dessa forma, 100 g de amostra contém -------- 0,1 g de enxofre
3º) Calculando:
0,1 g de enxofre ------ 100 g de amostra (barra de aço)
X ------- 200 g de amostra (barra de aço)
Portanto, X = 0,2 g de Enxofre, ou seja, em 200 g de aço, 0,2 g são de enxofre, a impureza desta amostra.
Após os grupos desenvolverem os cálculos referentes a massa de enxonfre na amostra, entregue a Atividade 1 impressa para cada grupo, disponível no link a seguir:
O gabarito da atividade pode ser acessado através do link:
Mão na massa

Orientações: Imprima uma cópia da Atividade 2 e entregue para cada grupo, podendo ser acessada através do link:
Permita que os grupos analisem e debatam sobre as questões abordadas a partir de dados tabelados. (tempo sugerido para a Atividade 2: 10 minutos)
O gabarito da atividade pode ser acessado através do link:
Sistematização

Tempo sugerido: 9 minutos
Orientações: Projete o slide ou escreva as questões da sistematização no quadro. Permita que os grupos reflitam e troquem ideias. Peça então para que cada um apresente suas respostas, tendo como base todas as atividades realizadas nesta aula. Espera-se que após todas as atividades, os alunos cheguem às seguintes conclusões:
1º) Uma substância que apresenta alto teor de pureza é aquela que apresenta uma porcentagem mínima de elementos ou substâncias contaminantes em suas estrutura (pequenas quantidades). Geralmente na Natureza não encontramos substâncias 100% puras, portanto quase todos os reagentes precisam ser purificados antes de utilizados. Quanto maior o grau de pureza de um reagente, maior o seu custo.
2º) Impurezas são substâncias que se encontram em pequenos quantidades e dispersos em uma substância de estrutura majoritária, e que em geral, não participam da transformação química desejada. As impurezas podem ocorrer naturalmente ou serem resultado da produção de uma substância em uma transformação química. Em geral, tantos os reagentes como os produtos das reações químicas precisam ser purificados.
3º) Cálculos de pureza de reagentes são importantes, pois através deles podemos determinar a quantidade real de massa dos produtos após uma reação química, assim como controlar a qualidade do produto. Como observado no contexto, uma espada de samurai necessita de pequenas porcentagens de carbono para se manter flexível e resistente (menos de 1%). Se essa a quantidade de carbono presente na liga for maior, ele passa a ser considerado uma impureza, pois prejudica a qualidade do aço e, portanto, da espada. Questões como esta são de extrema importância para a indústria química de todos os setores (metalúrgica, farmacêutica, petroquímica, alimentícia etc.), por isso os aspectos quantitativos das transformações químicas são tão importantes – eles nos permitem prever e calcular rendimentos, custos, energia produzida nas reações de combustão etc.
Sugestão de adaptação para ensino remoto
Ferramentas sugeridas
Essenciais:
- Videochamadas: Zoom ou Hangouts.
- Envio de mensagens e documentos: e-mail, Whatsapp ou Google Classroom.
Optativas: caso a turma disponha de tempo e de conexão síncrona de qualidade, os alunos podem construir a cadeia virtualmente, com o professor compartilhando as imagens em arquivos do Google Drive.
Contexto e questão disparadora
Peça para os estudantes lerem o texto presente nos slides "Contexto". Proponha que respondam como é feita a espada de um Samurai. Peça para eles refletirem sobre a questão disparadora:
- O que são impurezas?
Mão na massa
Divida a turma em cinco grupos e envie a atividade em Word, via Whatsapp.
Peça para responderem:
- O que torna uma substância pura?
- Qual a diferença entre pureza e impureza?
- Existem substâncias puras na Natureza?
Em seguida, analisem a tabela e respondam:
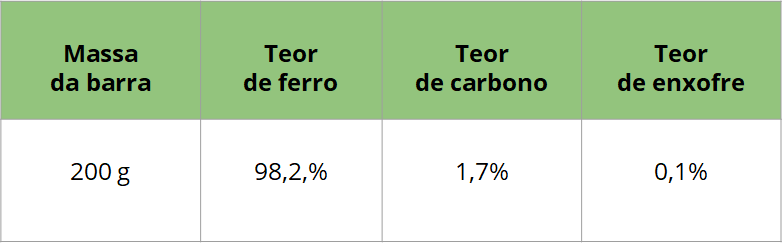
- Como você interpreta essa tabela? O que significam os valores em porcentagem?
- Como saber qual componente é a impureza do aço?
- Qual é o principal componente que constitui o aço?
Explique que eles podem trabalhar individualmente e, depois, se reunir com o grupo pelo Zoom ou pelo próprio Whatsapp.
Marque a data com os representantes dos grupos e peça para eles enviarem a atividade.
Material de apoio:
Link 1 (disponível aqui).
Link 2 (disponível aqui).
Sistematização
Marque uma videochamada com toda a turma pelo Google Meet. Proponha uma conversa e permita que os grupos reflitam e troquem ideias sobre substância pura.
Tutorial Google Meet (disponível aqui).
Convite às famílias
Os membros da família podem colaborar estimulando a execução das atividades.
Pureza de reagentes e produtos
9º ano
Objetivos de aprendizagem
Aplicar o conhecimento sobre as leis ponderais em um problema prático envolvendo pureza em materiais e nas transformações químicas.
Habilidade da Base Nacional Comum Curricular
(EFO9CI02) Comparar quantidades de reagentes e de produtos envolvidos em transformações químicas, estabelecendo a proporção entre suas massas.
Professor-autor: João Paulo Trindade dos Santos
Mentor: Denise Curi
Especialista: Leandro Holanda
Sobre esta aula: Para o pleno desenvolvimento desse plano, é essencial que os alunos tenham construído e desenvolvido habilidades
referente aos quatro planos anteriores, desta unidade, sobre as leis ponderais (Conservação das Massas e das Proporções Constantes), reações de combustão (rearranjo dos átomos durante uma reação química) e interpretação e balanceamento de equações químicas. Este plano é uma síntese das habilidades e conceitos desenvolvidos e aplicados para o fechamento desta unidade.
Este plano tem por objetivo possibilitar aos alunos que observem, a partir de tabelas e gráficos, a composição percentual dos componentes que são encontrados em materiais, substâncias e regentes de uma reação químicas. Ao fim deste planos os alunos deverão ser capazes de interpretar e identificar impurezas como componentes indesejados em uma amostra, comprometendo suas propriedades e, consequentemente, suas aplicações.
Para o desenvolvimento deste plano, serão realizadas duas atividades para impressão, que podem ser acessadas através dos links a seguir:
Atividade 1: <https://nova-escola-producao.s3.amazonaws.com/9W8gw6F5TR5n35kvZxHnFPeuTRWaK4WYHWzsJs8j2gvsntebUW2skXdjD9UN/cie9-02me05--atividade-para-impressao-1.pdf>.
Atividade 2: <https://nova-escola-producao.s3.amazonaws.com/W8NUXnET7PzvWJuQfaQGNMkxjVQf7SGJ6PZxfaAVSE4q7Zs8kBzEw55aefc8/cie9-02me05--atividade-para-impressao-2.pdf>.
O gabarito das atividades pode ser acessado através dos links:
Gabarito da atividade 1: <https://nova-escola-producao.s3.amazonaws.com/Jm3pqvW2EK3YtxU92GUMrBumy7RQBTQGsCfCrnj2HuwR56DDjQhUYjVh9kH7/cie9-02me05--gabarito-da-atividade-para-impressao-1.pdf>.
Gabarito da atividade 2: <https://nova-escola-producao.s3.amazonaws.com/AWUKn7PMTUZEmTY2wQm6RDZMq2hKERj83nGxFR7mqUZVgs26HW7D7rcZD4Qw/cie9-02me05--gabarito-da-atividade-para-impressao-2.pdf>.
Para estudar mais sobre o assunto, o professor pode acessar as seguintes referências:
FOGAÇA, Jennifer Rocha Vargas. “Cálculos estequiométricos com reagentes impuros”. Mundo Educação. Disponível em: <https://mundoeducacao.bol.uol.com.br/quimica/calculos-estequiometricos-com-reagentes-impuros.htm>. Acesso em 12 de agosto de 2018.
FOGAÇA, Jennifer Rocha Vargas."Aço"; Brasil Escola. Disponível em <https://brasilescola.uol.com.br/quimica/aco.htm>. Acesso em 12 de setembro de 2018.
MIODOWNIK, Mark. De que são feitas as coisas. Tradução de Marcelo Barbão. Editora Edgard Blücher Ltda., 2015. 34 p.